Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Промышленные способы получения оснований.Библиотека / Основания / Библиотека / Основания / Промышленные способы получения оснований. Промышленные способы получения оснований.Страница 1
Промышленные способы получения любых химических продуктов, а не только оснований, учитывают много различных факторов, среди которых можно выделить доступность реагентов, их токсичность и агрессивность при транспортировке, температуру процесса получения, необходимость применения катализаторов, легкость выделения из смеси. Поэтому для получения оснований реагенты должны быть легкодоступны и дешевы, не токсичны, температура процесса получения должна быть не слишком высокой, чтобы обойтись без использования дорогостоящих термостойких и кислотоупорных резин, футеровок.
В промышленных масштабах получают лишь несколько гидроксидов: NaOH, ROH, LiOH. Из них самый распространенный - NaOH. Рассмотрим методы получения гидроксида натрия NaOH в химической промышленности.
Для получения гидроксида натрия в химической промышленности используют электролиз. Электролитом выступает раствор хлорида натрия ( поваренной соли ). Во время электролиза через раствор электролита пропускают постоянный электрический ток и на электродах при этом проходят процессы окисления и восстановления.
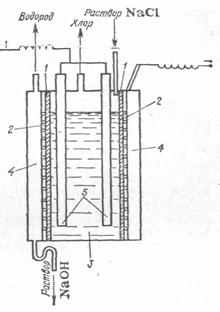 Электролиз раствора хлорида натрия с целью получения гидроксида натрия ведут двумя способами: на железном катоде и на ртутном катоде. Анодом в обоих случаях служит искусственный графит. Установка для промышленного получения гидроксидов натрия и калия приведена на рисунке 3. При электролизе по первому способу на катоде выделяется водород, а в прикатодном пространстве накапливается щелочь. На аноде выделяется хлор и частично кислород. Уравнения электродных реакций:
Электролиз раствора хлорида натрия с целью получения гидроксида натрия ведут двумя способами: на железном катоде и на ртутном катоде. Анодом в обоих случаях служит искусственный графит. Установка для промышленного получения гидроксидов натрия и калия приведена на рисунке 3. При электролизе по первому способу на катоде выделяется водород, а в прикатодном пространстве накапливается щелочь. На аноде выделяется хлор и частично кислород. Уравнения электродных реакций:
на катоде: ![]()
Рис. 3. на аноде: ![]()
Суммарное уравнение электролиза будет:
![]()
При электролизе по второму методу на ртутном катоде восстанавливается не водород, а натрий. Восстановление натрия возможно благодаря высокому перенапряжению разряда ионов водорода на ртути и образованию интерметаллического соединения натрия с ртутью (растворы металлов в ртути принято называть амальгамами). При этом потенциал восстановления натрия на ртути снижается до - 1,8В против ![]() на натрии.
на натрии.
На электродах протекают следующие реакции:
на катоде: ![]()
на аноде: ![]()
Тогда суммарная реакция процесса электролиза будет: ![]()
Амальгаму натрия затем разлагают водой. Натрий вступает в реакцию с водой с образованием щелочи и водорода, причем полученный таким способом гидроксид натрия отличается высокой чистотой.
Для электролиза применяют чистую поваренную соль. Ее предварительно очищают от ионов Са2+ действием соды и от ионов Мg2+ действием едкого натра; осадок углекислого кальция и гидроокиси магния отфильтровывают. Электролизу подвергают почти насыщенный раствор хлористого натрия (300 – 310 г/л соли) при 70 – 90°С. При такой концентрации и температуре электропроводность раствора высока, а растворимость хлора мала (не более 0,25 г/л), перенапряжение разряда ионов хлора минимально, а кислорода – максимально. При рН=7 ![]() ,
, ![]() . Поэтому анодную реакцию необходимо вести на таком электроде, на котором перенапряжение кислорода было бы более высоким, чем хлора. Этому требованию удовлетворяет графит.
. Поэтому анодную реакцию необходимо вести на таком электроде, на котором перенапряжение кислорода было бы более высоким, чем хлора. Этому требованию удовлетворяет графит.
Смотрите также
Радиоактивный анализ
Радиоактивный
анализ открыл в конце XIX столетия (в 1895 г.) немецкий физик Вильгельм Конрад Рентген невидимые
лучи способные беспрепятственно проходить через твёрдые тела и вызывать
почерн ...
Развитие химии высокомолекулярных соединений
...
Эволюционная химия - высшая ступень развития химических
знаний. Ближайшие перспективы химии
До недавнего
времени об эволюционной химии ничего не было известно. В отличие от биологов,
химиков не интересовал вопрос о «происхождении видов» вещества, потому что
получение любого ново ...


