Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Строение молекулы воды.Библиотека / Необычные свойства обычной воды / Библиотека / Необычные свойства обычной воды / Строение молекулы воды. Строение молекулы воды.
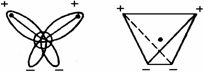
Молекула воды состоит из двух атомов водорода (Н) и одного атома кислорода (О). Все многообразие свойств воды и необычность их проявления в конечном счете определяются физической природой этих атомов и способом их объединения в молекулу. В отдельной молекуле воды ядра водорода и кислорода расположены так относительно друг друга, что образуют как бы равнобедренный треугольник со сравнительно крупным ядром кислорода на вершине и двумя мелкими ядрами водорода у основания. В молекуле воды имеются четыре полюса зарядов: два отрицательных за счет избытка электронной плотности у кислородных пар электронов и два положительных - вследствие недостатка электронной плотности у ядер водорода - протонов. Такая ассиметричность распределения электрических зарядов воды обладает ярко выраженными полярными свойствами; она является диполем с высоким дипольным моментом -1,87 дебай
Благодаря этому молекулы воды стремятся нейтрализовать электрическое поле. Под воздействием диполей воды на поверхности погруженных в нее веществ межатомные и межмолекулярные силы ослабевают в 80 раз. Столь высокая диэлектическая проницаемость из всех известных веществ присуща только воде. Этим объясняется ее способность быть универсальным растворителем.
Помогая" контактирующим с ней молекулам разлагаться на ионы (например, солям кислот), сама вода проявляет большую устойчивость. Из 1 млрд. молекул воды диссоциированными при обычной температуре оказываются лишь две, при этом протон не сохраняется в свободном состоянии, а вероятнее всего входит в состав иона гидроксония.
Вода химически не изменяется под действиям большинства тех соединений, которые она растворяет, и не изменяет их. Это характеризует ее инертным растворителем, что важно для живых организмов на нашей планете, поскольку необходимые их тканям питательные вещества поступают в водных растворах в сравнительно устойчивом виде. Как растворитель вода многократно используется, неся в своей структуре память о ранее растворенных в ней веществахВ такой модели углы между каждой парой линий, соединяющих центр (атом О) с вершинами, равны 109,5 С .
Смотрите также
Роль различных веществ в питании человека
...
Особенности гель-фильтрации
...
Нитрование n-нитроацетанилид
Нитрования – один
из важнейших процессов в химической промышленности. Продукты, получаемые за
счёт нитрования, являются полуфабрикатами для производства многих товаров
различных назначений ...


