Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Массовая доля растворенного вещества. Разбавление,
концентрирование и смешивание растворовCправочник по химии для подготовки к ЕГЭ / Решение расчетных задач / Cправочник по химии для подготовки к ЕГЭ / Решение расчетных задач / Массовая доля растворенного вещества. Разбавление,
концентрирование и смешивание растворов Массовая доля растворенного вещества. Разбавление,
концентрирование и смешивание растворовСтраница 1
Массовая доля растворенного вещества В
(ωв) – это отношение массы вещества В (тв) к массе раствора (m(р)):
![]()
При решении ωв выражается всегда в долях единицы (например, ωв = 0,01), в ответе – часто в процентах (ωв=1 %).
Величина, численно равная ωв (в %), характеризует раствор в целом, например, при ωв = 1 % раствор будет однопроцентным (1 %‑ный раствор вещества В).
Соотношения для массы раствора:
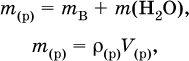
где ρ(р) – плотность и V(p) – объем раствора.
Для воды условно считается, что ее масса и объем численно
равны, т. е. плотность принимается равной 1 г/мл или 1000 г/л.
Если для приготовления раствора берется кристаллогидрат некоторой соли (а не сама безводная соль), то используются соотношения:
а) масса кристаллогидрата В хН2O
![]()
где m(кр. Н2O) – масса воды, которая содержится в данной массе кристаллогидрата;
б) масса безводной соли В в кристаллогидрате
![]()
так как nв = nкр;
б) масса добавляемой воды
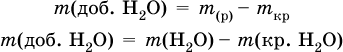
где т(Н2O) – суммарная масса воды в приготовленном растворе.
В лабораторной практике часто приходится готовить разбавленный
раствор вещества (величины с индексом ') из концентрированногораствора того же вещества (величины с индексом ") путем разбавления водой.
Масса растворенного вещества при разбавлении не изменяется:
![]()
Масса добавляемой воды определяется соотношением:
![]()
Для приготовления концентрированного раствора вещества В из разбавленного раствора применяют два способа.
а) Выпаривание некоторой порции воды из начального раствора. При этом масса растворенного вещества не меняется.
![]()
а масса воды, которую удаляют из раствора, определяется соотношением:
![]()
б) Добавление некоторой порции вещества В в начальный раствор. При этом масса воды не изменяется:
![]()
а масса добавленного вещества определяется соотношением
![]()
Для приготовления раствора с промежуточным составом
(величины без индексов) проводят смешивание концентрированногои разбавленного
растворов вещества В. При этом все величины связаны соотношениями:
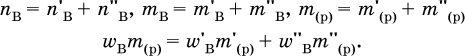
Примеры решения задач
1. Вычислите объем (в литрах, н.у.) аммиака, который полностью поглощается водой с образованием 500 г 20 %‑ного раствора.
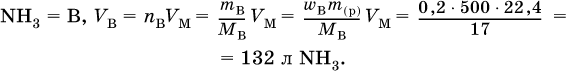
2. Какую массу (в граммах) кристаллогидрата Na2CO3 10Н2O следует использовать для приготовления 250 г 15 %‑ного раствора безводной соли?
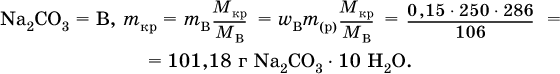
3. До какого объема (в литрах) надо разбавить водой 250 мл 30 %‑ного раствора нитрата аммония (плотность раствора 1,13 г/мл), чтобы приготовить 10 %‑ный раствор (плотность 1,04 г/мл)?
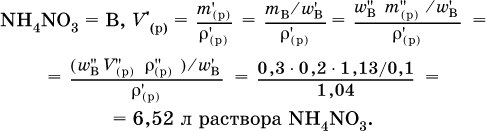
4. Установите массу (в граммах) выпаренной воды из 300 мл 4%‑ного раствора хлорида бария (плотность раствора 1033 г/л), если приготовлен 10 %‑ный раствор.
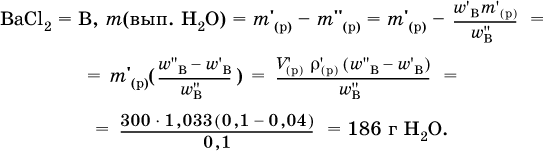
5. Вычислите массу (в граммах) порции гидроксида калия, которую добавили в 400 г 5%‑ного раствора этого вещества и довели массовую долю до 40 %.
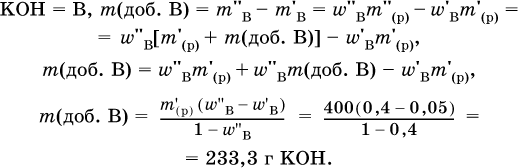
6. Определите массовую долю (в %) серной кислоты в конечном растворе, приготовленным смешиванием 90 г 5%‑ного и 120 г 40 %‑ного растворов этого вещества.
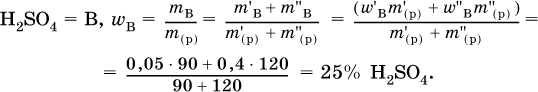
Задания для самостоятельного решения части В
1. Установите массовую долю (в %) хлорида калия в растворе, приготовленным из 0,65 моль соли и 300 мл воды.
2. Приготовлено 300 г 5%‑ного раствора иода в этаноле. Рассчитайте массу (в граммах) использованного спирта.
3. Какой объем (в литрах, н. у.) метаналя необходимо растворить в 500 мл воды, чтобы приготовить 30 %‑ный формалин.
Смотрите также
Химическая термодинамика
В
результате химической реакции выделяется или поглощается энергия, так как
реакция сопровождается перестройкой энергетических уровней атомов или молекул
веществ, участвующих в ней, и веще ...


