Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Реакции ионного обменаCправочник по химии для подготовки к ЕГЭ / Водные растворы. Растворимость и диссоциация веществ. Ионный
обмен. Гидролиз солей / Cправочник по химии для подготовки к ЕГЭ / Водные растворы. Растворимость и диссоциация веществ. Ионный
обмен. Гидролиз солей / Реакции ионного обмена Реакции ионного обмена
В разбавленных растворах электролитов (кислот, оснований, солей) химические реакции протекают обычно при участии ионов
. При этом все элементы реагентов могут сохранять свои степени окисления (обменные реакции) или изменять их (окислительно‑восстановительные реакции). Примеры, приводимые далее, относятся к обменным реакциям (о протекании окислительно‑восстановительных реакций см. разд. 14).
В соответствии с правилом Бертолле, ионные реакции протекают практически необратимо, если образуются твердые малорастворимые вещества
(они выпадают в осадок), легколетучие вещества(они выделяются в виде газов) или растворимые вещества – слабые электролиты(в том числе и вода). Ионные реакции изображаются системой уравнений – молекулярным, полным и кратким ионным. Ниже полные ионные уравнения опущены (читателю предлагается составить их самому).
При написании уравнений ионных реакций надо обязательно руководствоваться таблицей растворимости (см. табл. 8).
Примеры реакций с выпадением осадков:
а)
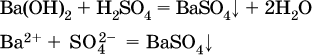
б)
![]()
в)
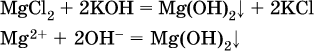
г)
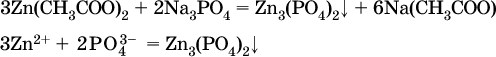
Внимание!
Указанные в таблице растворимости (см. табл. 15) малорастворимые («м») и практически нерастворимые («н») соли выпадают в осадок именно в том виде, как они представлены в таблице (СаF2↓, PbI2↓, Ag2SO4↓, AlPO4↓ и т. д.).
В табл. 15 не указаны карбонаты – средние соли с анионом CO32‑. Следует иметь в виду, что:
1) К2СO3, (NH4)2CO3 и Na2CO3 растворимы в воде;
2) Ag2CO3, ВаСO3 и СаСO3 практически нерастворимы в воде и выпадают в осадок как таковые, например:
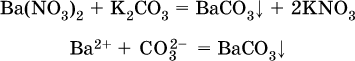
3) соли остальных катионов, такие как MgCO3, CuCO3, FeCO3, ZnCO3 и другие, хотя и нерастворимы в воде, но не осаждаются из водного раствора при проведении ионных реакций (т. е. их нельзя получить этим способом).
Например, карбонат железа (II) FeCO3, полученный «сухим путем» или взятый в виде минерала сидерит, при внесении в воду осаждается без видимого взаимодействия. Однако при попытке его получения по обменной реакции в растворе между FeSO4 и К2СO3 выпадает осадок основной соли (приведен условный состав, на практике состав более сложный) и выделяется углекислый газ:
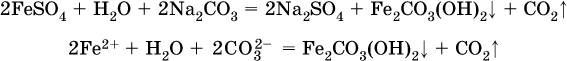
Аналогично FeCO3, сульфид хрома (III) Cr2S3 (нерастворимый в воде) не осаждается из раствора:
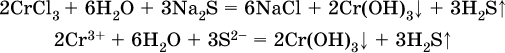
В табл. 15 не указаны также соли, которые разлагаютсяводой – сульфид алюминия Al2S3 (а также BeS) и ацетат хрома (III) Cr(СН3СОО)3:
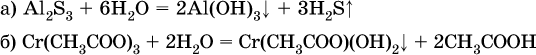
Следовательно, эти соли также нельзя получить по обменной реакции в растворе:
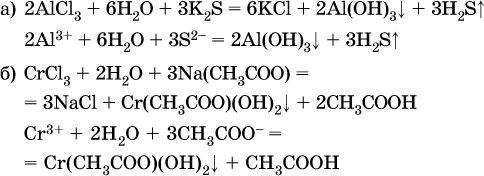
(в последней реакции состав осадка более сложный; подробнее такие реакции изучают в высшей школе).
Примеры
реакций с выделением газов:
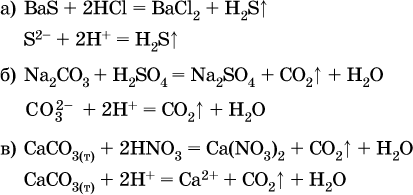
Примеры
реакций с образованием слабых электролитов:
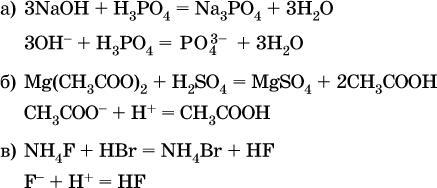
Если реагенты и продукты обменной реакции не являются сильными электролитами, ионный вид уравнения отсутствует, например:
![]()
Смотрите также
Катионы второй аналитической группы
...
Введение
Колебательные процессы играют существенную роль в
жизнедеятельности различных организмов, определяя основной механизм многих
явлений биологической подвижности (летательные мышцы насекомых, биение се ...
Неметаллы
Все многообразие окружающей нас природы
состоит из сочетаний сравнительно небольшого числа химических элементов.
В различные
исторические эпохи в понятие «элемент» вкладывался различный с ...


