Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Растворимость веществ в водеCправочник по химии для подготовки к ЕГЭ / Водные растворы. Растворимость и диссоциация веществ. Ионный
обмен. Гидролиз солей / Cправочник по химии для подготовки к ЕГЭ / Водные растворы. Растворимость и диссоциация веществ. Ионный
обмен. Гидролиз солей / Растворимость веществ в воде Растворимость веществ в водеСтраница 2
, в ненасыщенном растворе меньше
и в пересыщенном растворе большеего растворимости при данной температуре. Так, раствор, приготовленный при 20 °C из 100 г воды и сульфата натрия Na2SO4 (растворимость 19,2 г/100 г Н2O), при содержании
15,7 г соли – ненасыщенный;
19.2 г соли – насыщенный;
2O.3 г соли – пересыщенный.
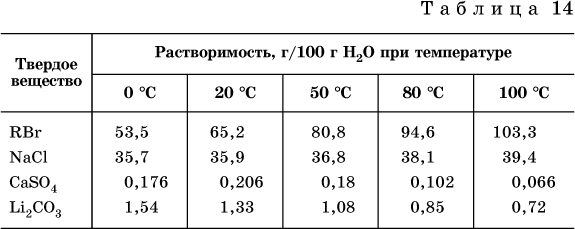
Растворимость твердых веществ (табл. 14) обычно увеличивается с ростом температуры (КBr, NaCl), и лишь для некоторых веществ (CaSO4, Li2CO3) наблюдается обратное.
Растворимость газов при повышении температуры падает, а при повышении давления растет; например, при давлении 1 атм растворимость аммиака составляет 52,6 (20 °C) и 15,4 г/100 г Н2O (80 °C), а при 20 °C и 9 атм она равна 93,5 г/100 г Н2O.
В соответствии со значениями растворимости различают вещества:
– хорошо растворимые, масса которых в насыщенном растворе соизмерима с массой воды (например, КBr – при 20 °C растворимость 65,2 г/100 г Н2O; 4,6М раствор), они образуют насыщенные растворы с молярностью более чем 0,1М;
– малорастворимые, масса которых в насыщенном растворе значительно меньше массы воды (например, CaSO4 – при 20 °C растворимость 0,206 г/100 г Н2O; 0,015М раствор), они образуют насыщенные растворы с молярностью 0,1–0,001М;
– практически нерастворимые, масса которых в насыщенном растворе пренебрежимо мала по сравнению с массой растворителя (например, AgCl – при 20 °C растворимость 0,00019 г на 100 г Н2O; 0,0000134М раствор), они образуют насыщенные растворы с молярностью менее чем 0,001М.
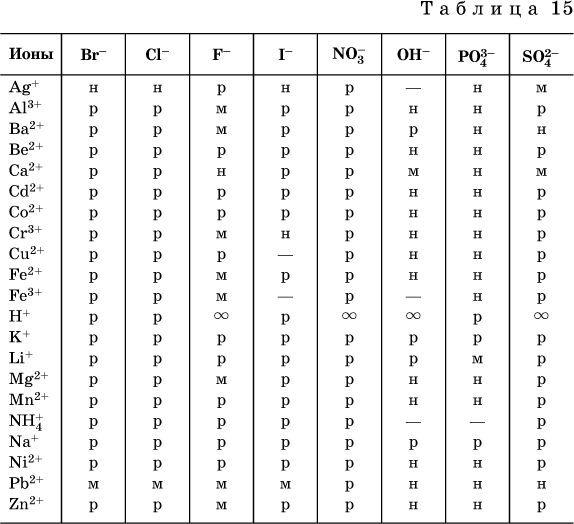
По справочным данным составлена таблица растворимости распространенных кислот, оснований и солей (табл. 15), в которой указан тип растворимости, отмечены вещества, не известные науке (не полученные) или полностью разлагающиеся водой.
Условные обозначения, используемые в таблице:
«р» – хорошо растворимое вещество
«м» – малорастворимое вещество
«н» – практически нерастворимое вещество
«–» – вещество не получено (не существует)
«![]()
» – вещество смешивается с водой неограниченно
Примечание. Данная таблица отвечает приготовлению насыщенного раствора при комнатной температуре путем внесения вещества (в соответствующем агрегатном состоянии) в воду. Следует учесть, что получение осадков малорастворимых веществ с помощью реакций ионного обмена возможно не всегда (подробнее см. 13.4).
Смотрите также
Постановка задачи
Целью данной работы являлась структурная и параметрическая
оптимизация технологической схемы разделения смеси
бензол-хлорбензол-дихлорбензол для снижения энергозатрат на разделение.
Для достижени ...
Анализ почв и агрохимический анализ
...
Йод
ИОД (лат. Iodium), I - химический элемент VII
группы периодической
системы Менделеева, относится к галогенам (в литературе
встречается также символ J); атомный номер 53, атомная масса 126, ...


