Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Экспериментальные методыСтатьи и работы по химии / Исследование растворимости и ионного обмена как инструмент изучения равновесий в водном растворе / Статьи и работы по химии / Исследование растворимости и ионного обмена как инструмент изучения равновесий в водном растворе / Экспериментальные методы Экспериментальные методы
Методы для определения растворимости в широких пределах экспериментальных условий были рассмотрены Циммерманом. При изучении равновесия в водном растворе изменение растворимости в зависимости от начального состава водной фазы измеряется при постоянной температуре.
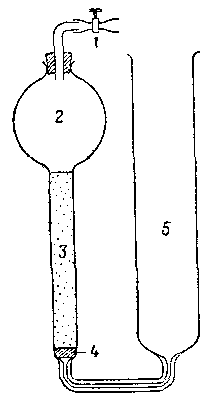
Рис. 1. Сатуратор Бренстеда — Дэписа.
1 – винтовой зажим, 2 – емкость, содержащая растворитель, 3 - колонка с тонкоразмельченным насыщающим твердым веществом; 4— пористая стеклянная прокладка; 5 - емкость, содержащая насыщенный раствор.
Равновесие между твердой фазой и раствором может быть достигнуто или встряхиванием в закрытом сосуде, или пропусканием водной фазы через сатуратор, наполненный твердым веществом; тип сатуратора, примененный Дэвисом и сотрудниками, показан на рис. 1. Равновесие следует устанавливать в термостате. Так как часто равновесие достигается медленно, следует проверять, получается ли одинаковое значение растворимости при ненасыщенной или пересыщенной начальной водной фазе, а также через различные промежутки времени. Равновесие в инертных системах [например, аммиакаты кобальта(Ш)] достигается быстрее с помощью катализатора. Иногда необходимо покрывать внутреннюю поверхность сосудов и пробок парафиновым воском или силиконом для того, чтобы избежать потерь растворенного вещества вследствие сорбции на стекле.
Твердая фаза может быть отделена от насыщенного раствора фильтрованием или центрифугированием, которые следует проводить при температуре равновесия. Особенно удобно помещение с постоянной температурой, но, если его нет, фильтрование можно легко выполнить в термостате. Например, установление равновесия и последующее разделение можно проводить в термостатированном сатураторе Дэвиса со встроенным фильтром. Если равновесие проводится в отдельных сосудах, то фазы могут быть разделены с помощью пипетки с пористым фильтром или термостатированного ультрафильтра Тиссена под давлением от 2 до 3 атм. Хотя и трудно проводить центрифугирование точно при температуре равновесия, если нет термостатирующего помещения, все же кристаллизацию из горячих растворов можно предотвратить продуванием горячего воздуха через центрифугу и с помощью подогретых пипеток для удаления водной фазы. Фазы могут иногда быть отделены более полно, если прокладка из ваты центрифугируется на поверхности твердого вещества.
Выбор аналитического метода в основном зависит от величины измеряемой растворимости. Умеренно высокие значения обычно определяют гравиметрическим или объемным методом, а низкие значения - полярографическим, колориметрическим или радиометрическим методами. Незаряженные формы могут быть иногда отделены от насыщенного раствора экстракцией. Так, растворимость углеводородных лигандов в водных растворах серебра (I) была определена спектрофотометрически после экстракции лиганда гексаном, в то время как растворимость дитизона в буферных растворах измерялась добавлением избытка радиоактивного серебра, экстрагированием дитизоната серебра хлороформом и определением активности в органической фазе.
Хотя измерение растворимости обычно включает анализ насыщенного раствора, были выполнены также эксперименты по смещению ряда растворов известной концентрации с последующим определением веса образовавшегося осадка.
Смотрите также
Закономерности образования и роста покрытий
...
Определение фенолов воде
Цель технического
отчета заключается в определении уровня загрязнения воды на очистных сооружениях
города Троицка.
Для выполнения
технического отчета я поставил перед собой следующие зад ...
Самоорганизация ион-проводящих структур при протекании электрохимических процессов на фазовых переходах, включающих серосодержащие компоненты
Актуальность темы
диссертации.
Тема диссертационной
работы относится к электрохимии твердого состояния, входящей как составная
часть в ионику твердого тела (ИТТ) -раздел науки, возникший ...


