Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Жидкофазное и газофазное гидрирование углеводородовСтатьи и работы по химии / Статьи и работы по химии / Жидкофазное и газофазное гидрирование углеводородов Жидкофазное и газофазное гидрирование углеводородовСтраница 4
Равновесие благоприятно для гидрирования неразветвленных углеводородов с небольшой молекулярной массой, а также для гидрирования низших олефинов, диенов и, как уже говорилось выше, для ацетиленовых углеводородов, причем наличие фенильных заместителей и разветвления углеродной цепи сказывается отрицательно. Менее выгодны условия гидрирования альдегидов, нитрилов, кетонов и ароматических ядер. Если провести сравнение для температуры, при которой Кр = 1, получим следующий ряд способности к гидрированию, учитывающий только термодинамические факторы:
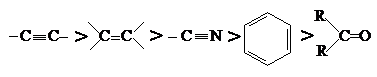
В процессах гидрирования, сопровождающихся выделением воды, равновесие обычно смещено вправо в большей мере, чем в других случаях.
Для гидрирования вещества Кр равна А + Н2 ® АН2
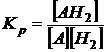 .
.
Для реакций перераспределения водорода А + ВН2 ® АН2 + В
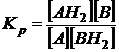
Равновесие реакции перераспределения будет смещено вправо, когда в термодинамическом отношении вещество А более склонно к гидрированию, чем вещество В, например:
3RCH=CH2 + C6H12 ® 3RCH2-CH3 + C6H6
Гидрирование может протекать в гомогенной (газовой или жидкостной), гетерогенной (газ-жидкость, газтвердое тело, жидкостьтвердое тело) системах в присутствии катализаторов или без них.
Скорость реакций гидрирования в общем случае может зависеть от диффузионных и кинетических факторов. Первые из них играют тем меньшую роль, чем интенсивнее перемешивание и чем ниже температура. Скорость гидрирования определяется в большей степени, чем для других процессов, влиянием следующих факторов:
· величиной окислительно-восстановительного потенциала системы;
· скоростью диффузии реагентов из одной фазы в другую;
· скоростями адсорбции, хемосорбции и диффузии в адсорбированный слой;
· ориентацией адсорбированных молекул и т.д.
Процессы гидрирования обычно осуществляются в условиях, когда равновесие реакции значительно смещено вправо и можно пренебречь обратной реакцией дегидрирования. Кроме того, насыщенный продукт гидрирования имеет небольшой адсорбционный коэффициент и поэтому обычно не входит в кинетическое уравнение процесса. И, наоборот, при высоком давлении становится существенной сорбция не только исходного вещества, но и водорода.
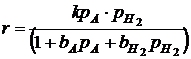 ,
,
где Р – парциальные давления реагентов;
b – адсорбционные коэффициенты реагентов.
С такими катализаторами, как платина, палладий, никель, энергично сорбирующими водород, скорость реакции при умеренных температурах (100оС) не зависит от парциального давления водорода. Оно начинает влиять на скорость только при повышении температуры - вначале незначительно, а затем пропорционально возрастанию давления. Наблюдается и отчетливое самоторможение реакции исходными ненасыщенными соединениями. Как уже говорилось, на оксидных катализаторах сорбция водорода менее значительна, чем на металлах, вследствие чего скорость обычно зависит от парциального давления водорода линейно. Этим обусловлена большая эффективность применения высоких давлений и избытка водорода при гидрировании на оксидных катализаторах.
Смотрите также
имическая сборка поверхности твердых тел путем молекулярного наслаивания
Получение принципиально новых характеристик
материалов и изделий, особенно при создании искусственных структур, основанных
на квантовых эффектах [1-6], невозможно в перспективе без создания ...


