Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Биокоординационные соединенияОткрытая химия / Биохимия / Открытая химия / Биохимия / Биокоординационные соединения Биокоординационные соединенияСтраница 1
Биокоординационные соединения выполняют важнейшие функции в растительных и животных организмах. Они в составе ферментов катализируют реакции переноса кислорода, окислительно-восстановительные и гидролитические процессы, чаще всего биокоординационные соединения представляют собой металлсодержащие макромолекулы. Связанный с белком металл может контролировать конформацию биомакромолекул. Так, Mg2+, Ca2+ стабилизируют двойную спираль ДНК, тогда как Cu2+ благоприятствует ее раскручиванию. В этом параграфе мы ограничимся некоторыми примерами биокоординационных соединений, ответственных, в частности, за фотосинтез, перенос кислорода, окислительно-восстановительные процессы.
Хлорофилл. Этим термином определяют группу магнийсодержащих пигментов, ответственных за процессы фотосинтеза. Наиболее распространенным является хлорофилл а, который содержится во всех растениях, образующих кислород в процессе фотосинтеза. Кроме него известны не менее восьми разновидностей.
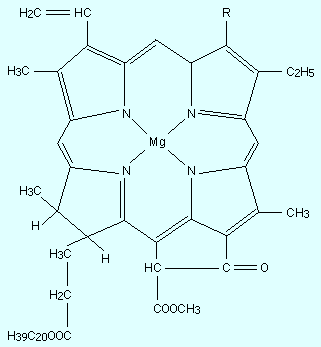
Хлорофилл а представлен на рис. 13.7.
 |
|
Рисунок 13.7 Молекула хлорофилла a |
В процессе фотосинтеза солнечная энергия поглощается хлорофиллом. Высвобождаемый кислород первоначально принадлежал воде. Водород восстанавливает фермент никотинамидадениндинуклеотид (НАД+), в результате чего образуются НАД∙H и H+, которые принимают участие в цикле синтеза углеводов. Эта стадия называется световой. Темновая стадия заключается во взаимодействии CO2 и H2O с рибулозодифосфатом с образованием двух молекул фосфоглицериновой кислоты: 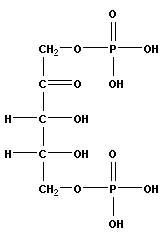 +
+ ![]() +
+ ![]() → 2
→ 2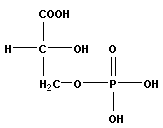
Фосфоглицериновая кислота присоединяет вторую фосфатную группу от аденозинтрифосфата (АТФ), а дифосфоглицериновая кислота восстанавливается с помощью НАД∙Н в фосфотриозу, участвующую в синтезе сахаров от C3 до C7. Продуктами этой стадии являются АТФ и фруктозофосфат, превращающийся в дальнейшем в глюкозу и крахмал.
Гемоглобин – гемсодержащий белок, обратимо связывающий молекулярный кислород (рис. 13.7):
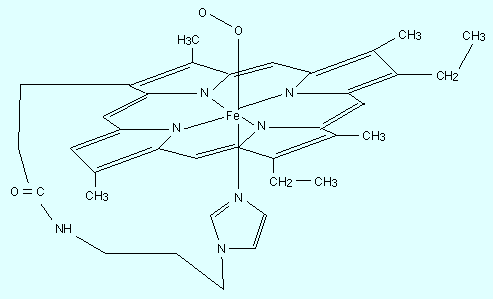
Из рис. 13.8 видно, что как и Mg2+ в хлорофилле, Fe2+ связан с четырьмя атомами азота пиррольных колец порфириновой системы (протопорфирина IX) и с атомами азота имидазольного кольца остатка аминокислоты – гистидина, входящего в состав полипептидной части гемоглобина. Шестое координационное место занимает дикислород или другие малые лиганды (CO в карбоксигемоглобине HbCO).
 |
|
Рисунок 13.8 Молекула гемоглобина |
Volkswagen ID.4 2021 года предлагает стильную и функциональную центральную консоль, которая объединяет передовые технологии и удобство. Чтобы ознакомиться с особенностями центральной консоли этого электромобиля, посетите страницу с обзором центральной консоли.
Центральная консоль ID.4 позволяет водителю и пассажирам иметь доступ к основным функциям автомобиля, таким как управление мультимедийной системой и настройками климата, обеспечивая комфорт и удобство во время поездки.
Смотрите также
Химические свойства ароматических углеводородов. Полиядерные ароматические соединения
Реакции электрофильного замещения:
галогенирование, нитрование, сульфирование, алкилирование, ацилирование.
Механизм реакции электрофильного замещения. Понятие о p- и s-комплексах, их строен ...
Олигосахариды и полисахариды
...
Переработка полимерных материалов
В настоящее время
предусматривается дальнейшее улучшение обслуживания населения страны всеми
видами транспорта, в том числе и железнодорожным транспортом. Решение этой
проблемы возможно не ...


