Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Гидролиз
солей сильных кислот и слабых основанийСтатьи и работы по химии / Гидролиз солей. Особенности почвенного гидролиза / Статьи и работы по химии / Гидролиз солей. Особенности почвенного гидролиза / Гидролиз
солей сильных кислот и слабых оснований Гидролиз
солей сильных кислот и слабых оснований
Реакцию гидролиза соли, образованной сильной кислотой и слабым основанием, схематически можно изобразить так:
![]() М+ + А - + Н2О МОН + Н+ +А - , (16) и константа гидролиза
М+ + А - + Н2О МОН + Н+ +А - , (16) и константа гидролиза
Кг = ![]() . (17)
. (17)
Раствор имеет кислую реакцию (Сн+>Сон-). Одним из продуктов гидролиза является слабое основание. Диссоциация слабого основания препятствует протеканию гидролиза до конца
![]() МОН М+ + ОН - ;
МОН М+ + ОН - ;
К осн. = ![]() ,
,
Откуда ![]() . (18)
. (18)
Подставив выражение (18) в (17), получим
Кг = ![]() .
.
Подобно выводу выражения (12), при гидролизе соли, образованной слабым основанием и сильной кислотой
a » ![]() . (19)
. (19)
Как и в первом случае, увеличение концентрации соли в воде приводит к уменьшению степени гидролиза a. Разбавление раствора увеличивает степень гидролиза. Подставив в уравнение (19) значение Кг, получим
a » 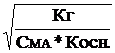 . (20)
. (20)
Степень гидролиза соли обратно пропорциональна корню квадратному из константы диссоциации слабого основания. Рассматривая гидролиз соли слабого основания и сильной кислоты, получим выражение, аналогичное уравнению (15)
РН = ½ рКw - ½рКосн. - ½ lgСМА. (21)
Из выражения (21) видно, что рН уменьшается с уменьшением Косн. и с увеличением Сма, или кислотность раствора возрастает с уменьшением константы диссоциации слабого основания и с ростом общей концентрации соли.
Смотрите также
Производство этилового спирта
Этиловый спирт находит широкое применение в народном хозяйстве в
качестве растворителя, также применяется в производстве дивинила, в пищевой и
медицинской промышленности, в качестве горючего ...
Термический анализ
Метод исследования
физико-химических и химических превращений, происходящих в минералах и горных
породах в условиях заданного изменения температуры. Термический анализ
позволяет идентифицировать от ...
Реакции a-литиированных циклических нитронов с электрофильными реагентами
...


