Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Галогены в природе. Получение галогенов.Статьи и работы по химии / Галогены / Статьи и работы по химии / Галогены / Галогены в природе. Получение галогенов. Галогены в природе. Получение галогенов.
Фтор встречается в природе в виде фторидов, например, флюорита CaF2. Фтор получают электролизом расплавов фторидов щелочных металлов. Для понижения температуры плавления электролизу подвергают кислые фториды состава KF. 2HF * ) , что позволяет проводить процесс при 1000С (Тпл. чистого KF составляет 8570С). Материалом для электролизера служат медь, никель или сталь, которые покрываются с поверхности плотной пленкой фторида, препятствующей дальнейшей коррозии реактора.
В лабораторных условиях фтор можно получить термолизом высших фторидов некоторых металлов, например,
2CeF4 = 2CeF3 + F2 .
Хлор встречается в природе, в основном, в виде хлоридов. Например, известны мощные залежи галита (NaCl), образовавшиеся при испарении соленых морей и озер. Основным методом получения хлора из галита является электролиз концентрированного раствора NaCl с диафрагмой, разделяющей катодное и анодное пространства:
2NaCl + 2H2O 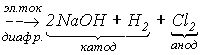
В лабораторных условиях хлор получают взаимодействием концентрированной HCl с такими окислителями, как КMnO4 , а также MnO2, K2Cr2O7 и т.д.
16HCl + 2KMnO4 = Cl2 +2KCl +2MnCl2 + 8H2O.
Реакция твердого KMnO4 с концентрированной HCl протекает с образованием темно-коричневого малорастворимого гексахлороманганата (IV) калия и раствора, содержащего хлоридные комплексы Mn(III):
![]()
Полное восстановление KMnO4 до MnCl2 осуществляется при большом избытке HCl.
Бром, содержащийся в морской воде и буровых водах в виде бромидов, извлекают путем обработки реакционной смеси хлором при рН=3.5, чтобы избежать образования солей оксокислот брома.
Аналогичным образом из буровых вод и золы, образующейся при сгорании морских водорослей, выделяют иод.
В лаборатории бром и иод получают взаимодействием галогенидов с окислителем (MnO2) в кислой среде, например:
MnO2 + 2H2SO4 + 2KI = I2 + MnSO4 + 2H2O + K2SO4
Образующийся йод экстрагируют или отделяют перегонкой с водяным паром.
Смотрите также
Изоляция космических кораблей
...
Получение уксусной кислоты
...
Метод суспензионной полимеризации винилхлорида
Термопластичный
полимер поливинилхлорид (ПВХ) – твердое вещество белого цвета, являющееся
продуктом полимеризации винилхлорида, выпускается в виде сыпучего порошка,
готового для дальнейшей ...


