Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Осмотическое давление растворов ВМС.Статьи и работы по химии / Высоко-молекулярные соединения / Статьи и работы по химии / Высоко-молекулярные соединения / Осмотическое давление растворов ВМС. Осмотическое давление растворов ВМС.
Согласно уравнению Вант – Гоффа осмотическое давление растворов увеличивается прямо пропорционально концентрации. Для ВМС эксперимент показывает, что осмотическое давление значительно выше чем это требуется по закону Вант – Гоффа.
Чем более гибка молекула, тем при прочих равных условиях осмотическое давление выше и тем больше оно отклоняется от значения, вычисленного по уравнению Вант – Гоффа. Для описания зависимости осмотического давления предложено уравнение
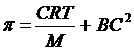 |
или
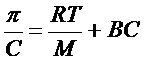 |
Где С – концентрация, М – относительная молекулярная масса полимера, В – некоторый коэффициент характеризующий отклонение от уравнения Вант – Гоффа.
Смотрите также
Исследование возможностей синтеза фенилселиконатов натрия, содержащих в своем составе атом кобальта
Министерство образования и науки Российской
Федерации
Федеральное государственное автономное образовательное
учреждение
Дальневосточный Федеральный Университет
Институт химии и прик ...
Химия актиноидов (актинидов)
...
Марказит
Название происходит от
арабского "marcasitae", которым алхимики обозначали соединения серы,
в том числе и пирит. Другое название - "лучистый колчедан".
Спектропиритом назван за ...


