Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Обсуждение результатов. Исследование гетерогенных катализаторов
амидирования м-толуиловой кислоты. Термодинамика процессаДипломы, курсовые и прочее / Выбор катализатора амидирования и изучение в его присутствии превращения м-толуиловой кислоты в N,N-диэтил-м-толуамид / Дипломы, курсовые и прочее / Выбор катализатора амидирования и изучение в его присутствии превращения м-толуиловой кислоты в N,N-диэтил-м-толуамид / Обсуждение результатов. Исследование гетерогенных катализаторов
амидирования м-толуиловой кислоты. Термодинамика процесса Обсуждение результатов. Исследование гетерогенных катализаторов
амидирования м-толуиловой кислоты. Термодинамика процесса
Поскольку реакция амидирования м-толуиловой кислоты (МТК) является обратимой, на первом этапе исследований были изучены термодинамические характеристики процесса. С целью определения состава равновесной смеси и условий, при которых могут быть сняты термодинамические ограничения, на первых порах был проведен расчет констант равновесия при различных температурах в диапазоне 260-320°С для реакции (табл. 3.1).
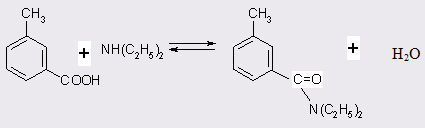
толуамид катализатор кислота токсикологический
Расчет констант равновесия проводился по экспериментальным данным после достижения в статических условиях устойчивых равновесных концентраций компонент [51]. В качестве катализатора реакции в данном случае использовали 0,5 мас.% хлорной кислоты. Достижение равновесия при любых температурах определялось только с одной стороны (опыты по гидролизу диэтилтолуамида не проводились).
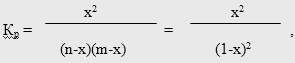
где х - степень превращения МТК или ее мольная доля [52]; n и m - мольные доли исходных компонентов (для простоты принято, что n = m = 1).
Обработка полученных значений Кр по методу наименьших квадратов [53] позволила аппроксимировать их следующим эмпирическим уравнением:
Кр = exp(8,81 – 3019,25/Т),
которое, в частности, может быть использовано при синтезе химико-технологических систем на стадии проектирования.
Расчет термодинамически возможной степени превращения при различных температурах и мольных отношениях реагентов осуществлялся по формуле [51]
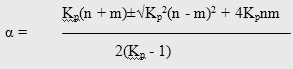
Таблица 3.1 Расчетные значения констант равновесия и термодинамически возможные степени превращения м-толуиловой кислоты при различных условиях синтеза м-ДЭТА
|
t, 0С |
К |
Соотношение МТК:диэтиламин |
Кр |
Степень превращения МТК (α) |
|
260 |
533 |
1:1 1:5 |
21,49 |
0,549 0,880 |
|
280 |
553 |
1:1 1:2 1:5 |
27,96 |
0,840 0,967 0,990 |
|
300 |
573 |
1:1 1:3 1:5 |
36,00 |
0,857 0,986 0,990 |
|
320 |
593 |
1:1 1:2 1:3 1:5 |
40,35 |
0,860 0,970 0,988 0,990 |
Анализ данных, представленных в табл. 3.1, позволяет сделать вывод, что при соотношении МТК: диэтиламин 1:1 мольн. и при 2600С термодинамически возможная степень превращения составляет 0,55, а при 320 0С - 0,86. При температуре 280 0С и мольном соотношении реагентов 1:2 термодинамические ограничения практически снимаются.
Отметим, что небольшие значения констант равновесия свидетельствуют о том, что, несмотря на снятие термодинамических ограничений, реакция по-прежнему остается равновесной. Поэтому дальнейшее увеличение концентрации диэтиламина и повышение температуры максимально благоприятствуют процессу.
Следующей важной характеристикой процесса является тепловой эффект реакции, который из-за отсутствия в литературе термодинамических характеристик исходных и конечных компонент (кроме диэтиламина и воды) был оценен по теплотам сгорания органических соединений в газообразном состоянии, и его величина составила ΔНо298= -20±5 кДж/моль. В свою очередь теплоты сгорания веществ, принимающих участие в реакции, рассчитаны по формуле [54]:
ΔНсгор= - (204,2n + 44,4m + Σх),
где n - число атомов кислорода, необходимое для полного сгорания вещества; m - число молей образующейся воды; х - поправка (термическая характеристика), постоянная в пределах гомологического ряда.
Термическая характеристика (х) - это фактически инкремент численных значений группы атомов или типа связи. Так, например, для МТК х = 100,4 кДж/моль [54]. Таким образом, выполненный термодинамический расчет показал возможность количественного превращения м-толуиловой кислоты в м-ДЭТА и позволил определить область режимов проведения реакции, соответствующих достижению поставленной цели.
Смотрите также
Методики анализа витаминов
...
Определение константы скорости реакции k по первым 3-м опытам
Из вида кинетического уравнения следует, что его единственным параметром
является константа скорости реакции k. Для
определения значения константы скорости воспользуемся статистическим методом
регр ...
Эпитаксиальный рост Ge на поверхности Si(100)
С физикой
тонких пленок связаны достижения и перспективы дальнейшего развития
микроэлектроники, оптики, приборостроения и других отраслей новой техники.
Успехи микроминиатюризации электронн ...


