Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Экспериментальная частьСтатьи и работы по химии / Акридон. Его получение, свойства и применение / Статьи и работы по химии / Акридон. Его получение, свойства и применение / Экспериментальная часть Экспериментальная часть
Реагенты и оборудование.
Уравнение реакции имеет вид:
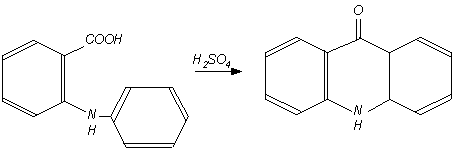
Реактивы: N-фенилантраниловая кислота (С13Н11О2N, M=213 г/моль, Тпл=179-1810С) – 3г, серная кислота (Н2SО4, M=98.08 г/моль, Тпл=-13.60С, Ткип=301,30С, плотность ρ=1,85, концентрация – 0,96%) – 7мл. Карбонат натрия – 2,12г (0,02моль). Вода.
Теоретический выход вещества по взятому в недостатке реактиву, участвующему в реакции (N-фенилантраниловая кислота) составляет 2,4г.
Схема прибора:
Методика эксперимента. В круглодонной колбе емкостью 50мл приготовлен раствор 3г N-фенилантраниловой кислоты в 7мл серной кислоты (98%) и раствор нагревался на кипящей водяной бане в течение 4-х часов, после чего его вылили в 100мл кипящей воды. Раствор приливали по стенке сосуда. В течение 5мин кипятили смесь, затем желтый осадок отфильтровали, сохранив фильтрат. Влажный осадок прокипятили в течение 5мин с раствором 2,12г (0,02 моль) соды в 30мл воды, после чего его отсосали с помощью водоструйного насоса, колбы Бунзена и воронки Бюхнера и хорошо промыли водой. Затем влажный осадок был высушен на воздухе. Выход вещества составил 1,78г или 74% от теоретического. Измеренная точка плавления вещества составила примерно 3440.
Смотрите также
Технология нуклеофильного замещения функциональных групп в органических соединениях
Атом
галогена в молекуле органического соединения с успехом может быть замещен на
другие группы атомов, что создает широкие возможности для синтеза биологически
активных соединений, исходя ...
О-хлорстирол
...
Зарождение химии
Представления древнегреческих
натурфилософов оставались ос-новными идейными истоками естествознания вплоть
до XVIII в. До начала эпохи Возрождения в науке господствовали представления
А ...


