Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Окислительно-восстановительные реакции органических веществДипломы, курсовые и прочее / Дипломы, курсовые и прочее / Окислительно-восстановительные реакции органических веществ Окислительно-восстановительные реакции органических веществСтраница 5
Ответ: Скорость реакции увеличится в 27 раз.
222. Как повлияет на выход хлора в системе :
4 HCl(г) + О2(г) « 2 Cl2(г) + 2 Н2О(ж), Q = 202,4 кДж,
а) повышение температуры в системе,
б) уменьшение общего объема смеси,
в) уменьшение концентрации кислорода,
г) увеличение общего объема реактора,
д) введение катализатора?
Решение:
4HCl(г) + О2(г) « 2Cl2(г) + 2Н2О(ж), Q = 202,4 кДж
Прямая реакция происходит с выделением тепла, т.е. является экзотермической (Q > 0), следовательно, обратная реакция будет протекать с поглощением тепла, т.е. является эндотермической (Q < 0). Согласно принципу Ле Шателье, если на систему, находящуюся в равновесии, воздействовать извне, изменяя какое-нибудь из условий (температура, давление, концентрация), то равновесие смещается таким образом, чтобы компенсировать изменение.
а) повышение температуры в системе будет способствовать сдвигу равновесия в сторону реакции, протекающей с поглощением тепла (эндотермической), т.е. в сторону реакции образования исходных веществ – выход хлора при этом уменьшится.
б) уменьшение общего объема смеси приведет к смещению равновесия в сторону реакции, протекающей с образованием меньшего числа молей газообразных веществ, т.е. в сторону прямой реакции – выход хлора при этом увеличится.
в) при уменьшении концентрации кислорода равновесие сдвигается в направлении образования исходных веществ – выход хлора при этом уменьшится.
г) при увеличении общего объема реактора давление в системе уменьшится, потому равновесие сдвинется в сторону увеличения числа газовых молей, т.е. в сторону обратной реакции – выход хлора при этом уменьшится.
д) катализатор одинаково ускоряет как прямую, так и обратную реакции и поэтому на смещение равновесия влияния не оказывает, а только способствует более быстрому его достижению, поэтому введение катализатора на выход хлора не повлияет.
237. Составьте схему, напишите уравнения электродных процессов гальванического элемента, у которого один электрод цинковый с концентрацией ионов цинка 10-2 моль/л, а второй – водородный с концентрацией ионов водорода 10-2 моль/л. Рассчитайте э.д.с. этого элемента.
Решение:
Схема химической цепи:
поток электронов
![]()
![]()
Электрод восстановитель (донор электронов) Электрод окислитель (акцептор электронов
![]()
где ![]() и
и ![]() – соответственно потенциалы положительного и отрицательного электродов.
– соответственно потенциалы положительного и отрицательного электродов.
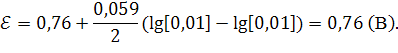
Ответ: Э.Д.С. равно ![]() .
.
262. Напишите уравнения реакций процессов, протекающих на электродах при электрохимической защите стальных труб.
Решение:
Одним из вариантов электрохимической защиты стальных труб есть протекторная защита. Если в качестве протектора взять цинк, то уравнения реакций процессов, протекающих на электродах будут следующие:
Смотрите также
Атомы и молекулы
Любое вещество состоит из ничтожно малых частиц – так называемых атомов. Часто атомы объединяются в группы, которые называют молекулами. Размеры атомов настолько малы, что увидеть их через обычн ...
История открытия и подтверждения периодического закона Д.И. Менделеева
Периодический
закон Д.И. Менделеева – это фундаментальный закон, устанавливающий
периодическое изменение свойств химических элементов в зависимости от
увеличения зарядов ядер их атомов ...
Полимерные сорбенты для распределительной хроматографии
Ограниченный
рабочий диапазон рН и сорбционная активность остаточных силанольных групп
сорбентов на основе силикагеля стимулировали разработку полимерных сорбентов
для распределительной хро ...


